
Журнал "Медицинский совет" №19/2022
DOI: 10.21518/2079-701X-2022-16-19-21-28
Т.Е. Таранушенко1,2, ORCID: 0000-0003-2500-8001
Н.А. Паршин1,2, ORCID: 0000-0002-7991-1063
А.А. Ваганов1,2, ORCID: 0000-0001-6032-6035
Т.В. Овчинникова2, ORCID: 0000-0002-9319-2894
1 Красноярский государственный медицинский университет имени профессора В.Ф. Войно-Ясенецкого; 660022, Россия, Красноярск, ул. Партизана Железняка, д. 1
2 Красноярский краевой клинический центр охраны материнства и детства; 660074, Россия, Красноярск, ул. Академика Киренского, д. 2а/1
Введение. Внутриутробная гипоксия и асфиксия при родах являются ведущими причинами младенческой смертности в структуре отдельных состояний, возникающих в перинатальном периоде.
Цель – изучить причастность негативных событий для плода в анте- и интранатальных периодах к возникновению перинатальной асфиксии у новорожденных и обозначить главные модифицируемые факторы риска, которые позволят сформулировать превентивные стратегии в развитии гипоксии ребенка.
Материалы и методы. Проведен ретроспективный анализ 50 историй болезни новорожденных за 2019–2020 гг.: проведена ретроспективная оценка течения анте- и интранатального периода. Проверка на нормальность распределения определила дальнейшие расчеты с использованием методов непараметрической статистики. Номинальные данные представлены с указанием абсолютных и относительных значений. Совокупности количественных показателей описаны значениями медианы (Me) и нижнего и верхнего квартилей (Q1–Q3). Для сравнения несвязанных выборок использовался критерий χ2.
Результаты. В группе детей с умеренной и тяжелой асфиксией при рождении преобладали недоношенные дети. Достоверность различий при сравнении сроков гестации между группами не отмечена, но при оценке медианы и квартилей наблюдается тенденция к более низкому сроку гестации в группе детей с тяжелой асфиксией. Основные анте- и интранатальные факторы риска асфиксии новорожденных установлены в следующем процентном отношении: фетоплацентарная недостаточность – 32%; преждевременный разрыв плодных оболочек и медицинские аборты в анамнезе – по 30%; первая беременность, анемия, ожирение, гипертоническая болезнь, курение, возраст матери > 35 лет – по 18%; истмико-цервикальная недостаточность – 16%; антенатальная гибель в анамнезе, угроза прерывания беременности, вагинит – по 14%; острые респираторные инфекции в период беременности, вспомогательные репродуктивные технологии (ЭКО), миома матки – по 12%; маловодие – 8%; многоводие – 6%.
Заключение. Структура факторов, способных вносить вклад в развитие асфиксии у новорожденных, разнообразна и включает как управляемые, так и неуправляемые влияния. Понимание причастности модифицируемых факторов риска определяет необходимость выстраивания стратегии и тактики по снижению их влияния на развитие рассматриваемой патологии.
Для цитирования: Таранушенко Т.Е., Паршин Н.А., Ваганов А.А., Овчинникова Т.В. Факторы риска развития асфиксии при рождении. Медицинский совет. 2022;16(19):21–28. https://doi.org/10.21518/2079-701X-2022-16-19-21-28.
Конфликт интересов: авторы заявляют об отсутствии конфликта интересов.
Risk factors for birth asphyxia
Tatiana E. Taranushenko1,2, ORCID: 0000-0003-2500-8001
Nikita A. Parshin1,2, ORCID: 0000-0002-7991-1063
Anatoliy A. Vaganov1,2, ORCID: 0000-0001-6032-6035
Tatiana V. Ovchinnikova2, ORCID: 0000-0002-9319-2894
1 Krasnoyarsk State Medical University named after Professor V.F. Voino-Yasenetsky; 1, Partizan Zheleznyak St., Krasnoyarsk, 660022, Russia
2 Krasnoyarsk Regional Clinical Center for Maternal and Child Health; 2a/1, Academician Kirensky St., Krasnoyarsk, 660074, Russia
Introduction. Intrauterine hypoxia and asphyxia during childbirth are the leading causes of infant mortality in the structure of certain conditions arising in the perinatal period.
Purpose. To study the involvement of negative events for the fetus in the ante- and intranatal periods in the occurrence of perinatal asphyxia in newborns and identify the main modifiable risk factors that will allow formulating preventive strategies in the development of child hypoxia.
Materials and methods. A retrospective assessment of the course of the anteand intranatal period was carried out according to 50 case histories. Nominal data are presented with indication of absolute and relative values. Sets of quantitative indicators are described by the values of the median (Me) and the lower and upper quartiles (Q1–Q3). The χ2 test was used to compare unrelated samples. Differences were considered statistically significant at p < 0.05. Statistical data processing was carried out using the Microsoft Office 2021 software package.
Results. In the group of children with moderate and severe asphyxia at birth, the median gestational age was 36 and 33 weeks. The main ante- and intranatal risk factors for asphyxia of newborns were established in the following percentage: fetoplacental insufficiency – 32%; premature rupture of membranes and medical abortions in history, 30% each; first pregnancy, anemia, obesity, hypertension, smoking, maternal age > 35 years, 18% each; isthmic-cervical insufficiency – 16%; history of antenatal death, threatened miscarriage, vaginitis, 14% each; acute respiratory infections during pregnancy, assisted reproductive technologies (IVF), uterine fibroids – 12% each; oligohydramnios – 8%; polyhydramnios – 6%.
Conclusion. The structure of factors that can contribute to the development of asphyxia in newborns is diverse. Understanding the involvement of modifiable risk factors determines the need to build a strategy and tactics to reduce their impact on the development of the pathology under consideration.
For citation: Taranushenko T.E., Parshin N.A., Vaganov A.A., Ovchinnikova T.V. Risk factors for birth asphyxia. Meditsinskiy Sovet. 2022;16(19):21–28. (In Russ.) https://doi.org/10.21518/2079-701X-2022-16-19-21-28.
Conflict of interest: the authors declare no conflict of interest.
Введение
Асфиксия новорожденных в наиболее простом определении означает неспособность ребенка начать самостоятельное дыхание после рождения. С позиции механизмов развития патологии и отдельных проявлений асфиксия является состоянием нарушенного газообмена, которое приводит к прогрессирующей гипоксии, гиперкапнии и ацидозу разной степени тяжести (в зависимости от причин и продолжительности развившейся ситуации). Ухудшение газообмена может произойти в анте-, интра- или раннем неонатальном периоде (если новорожденный не в состоянии поддерживать собственный газообмен без плаценты). Перинатальная асфиксия относится к значимым причинам неонатальной заболеваемости и смертности.
Термин «асфиксия при рождении» предложен Всемирной организацией здравоохранения как клиническое описание новорожденного, который «не может инициировать или поддерживать регулярное дыхание при рождении». Этот термин не раскрывает причинность данного состояния, так как причины нарушения или отсутствия дыхания у новорожденного могут быть различные (например, обусловленные недоношенностью).
В Международной классификации болезней 10-го пересмотра (МКБ-10) основным критерием диагноза «асфиксия» является оценка по шкале Апгар на 1-й минуте после рождения:
- тяжелая асфиксия (Р21.0) при сумме баллов 0–3 через 1 мин после рождения;
- средняя и умеренная асфиксия при рождении (Р21.1) при сумме баллов 4–7.
Несмотря на то что сумма 7 баллов через 1 мин после рождения соответствует асфиксии средней и умеренной тяжести, выставлять этот диагноз нецелесообразно, так как оценка 7 баллов по Апгар к концу 1-й минуты клинически и (или) прогностически малозначима. Многочисленные исследования указывают на то, что первая оценка по шкале Апгар слабо коррелирует c прогнозом и дальнейшим исходом у детей.
Для постановки диагноза «тяжелая асфиксия при рождении» предлагается использовать совокупность признаков:
- признаки внутриутробного или интранатального страдания плода;
- низкая оценка по шкале Апгар (< 5 баллов на 5-й минуте);
- рН < 7,0 или дефицит оснований (ВЕ) – > 16 ммоль/л в пуповинной крови;
- полиорганная недостаточность в раннем неонатальном периоде;
- неврологические нарушения с момента рождения [1].
К основным причинам внутриутробного неблагополучия плода относятся:
- хроническая гипоксия плода в течение нескольких недель или месяцев (наиболее распространенное последствие осложненной беременности, возникающее в результате повышенного сопротивления сосудов плаценты);
- хроническая плацентарная недостаточность как состояние, при котором происходит ремоделирование сосудов плаценты, нарушение маточно-плацентарного кровотока, прогрессирующее ухудшение функционирования плаценты, снижение поступления кислорода и питательных веществ к плоду через плаценту, что приводит к гипоксии и ацидозу плода.
Наиболее частыми последствиями этих состояний для плода являются задержка внутриутробного развития, недоношенность или антенатальная гибель плода [2]. Наряду с этим плацентарная недостаточность предрасполагает к акушерским расстройствам (преэклампсия, преждевременные роды, патологическое течение родов и др.), которые относят к основным причинам асфиксии, перинатальной заболеваемости и смертности во всем мире [2–4].
Отягощенный акушерский и соматический анамнез матери также могут внести существенный негативный вклад в развитие последующей асфиксии. Так, преэклампсия, гестационная или эссенциальная артериальная гипертензия, врожденные пороки сердца (цианотические), повышение внутрибрюшного давления (ожирение, многоводие), гестационный сахарный диабет, заболевания сосудов, хроническая бронхо-легочная патология (хроническая обструктивная болезнь легких, астма, интерстициальные болезни легких), многоплодная беременность, курение, наркозависимость, алкоголизм, анемии и другие заболевания крови с нарушением транспорта кислорода, воспалительные заболевания во время беременности, аутоиммунные заболевания у матери, тромбофилии, низкая масса тела матери, возраст матери, неблагоприятное экологическое окружение (высокий процент окиси углерода) и др. могут быть факторами риска хронической внутриутробной гипоксии и асфиксии при рождении [4, 6–11].
Важным модифицируемым фактором риска развития асфиксии является курение. Анализ формы допплеровских волн в различных плацентарных сосудах матерей, которые курили сигареты во время беременности, показал снижение высоты волны, а, следовательно, скорости кровотока, что указывает на воздействие никотина, приводящего к снижению маточно-плацентарного кровотока [12].
Острая респираторная вирусная инфекция (ОРВИ), перенесенная во время беременности, также является неблагоприятным фактором риска. Во время беременности увеличенная матка поднимает диафрагму до 4 см в III триместре и ограничивает функциональную остаточную емкость легких на фоне повышенной потребности в кислороде (в среднем на 20%). В случаях респираторной патологии наступает прогрессирование гипоксии у матери, а в последующем присоединяется внутриутробная гипоксия плода [6, 13]. Активно обсуждается вопрос об инфекции COVID-19 у матери как фактора риска асфиксии. В систематическом обзоре 2020 г. сообщается о результатах течения беременности и состоянии новорожденных от женщин, инфицированных COVID-19. Обзор включил 18 исследований из различных центров. Клинические характеристики течения COVID-19 у беременных и небеременных женщин схожи, значимых влияний инфекции на плод и новорожденных не установлено, но авторы отмечают необходимость дальнейшего наблюдения беременных, инфицированных в III триместре, для уточнения отсроченных влияний инфекции на ребенка [14].
Острая гипоксия плода с последующей асфиксией возникает на поздних сроках беременности. Причинами этого состояния чаще всего являются отслойка плаценты или тромбоз доли плаценты. Признаки гипоксии у плода появляются при утрате функции 1/3 плаценты [15]. К причинам, приводящим к острой гипоксии плода в интранатальном периоде, относят нарушение кровотока через пуповину (компрессия пуповины, сокращения пуповины во время родов, узлы пуповины, разрыв сосудов пуповины при оболочечном прикреплении, выпадение петель пуповины), отслойку плаценты, расстройство маточно-плацентарного кровотока (контрактуры миометрия, короткий интервал между сокращениями матки, дискоординация родовой деятельности, чрезмерно сильная родовая деятельность, тетанус матки), а также осложнения второго периода родов, когда происходит патологическое вставление плода (дистоция плечиков) и (или) имеют место переношенность, многоплодная беременность, общая анестезия матери [15, 16].
Представленные данные свидетельствуют об асфиксии как основной причине заболеваемости и смертности новорожденных детей, указывают на значительное разнообразие причин, способных инициировать развитие асфиксии у новорожденного. Вместе с тем структурированные исследования, позволяющие установить наиболее значимые факторы риска, малочисленны и разнообразны. Учитывая частоту встречаемости и наличие множества работ схожего формата, требуются дальнейшие современные исследования факторов риска и оценка их клинической значимости в развитии асфиксии.
Цель настоящего исследования – изучить причастность негативных событий для плода в антеи интранатальных периодах к возникновению перинатальной асфиксии у новорожденных и обозначить главные модифицируемые факторы риска, которые позволят сформулировать превентивные стратегии в развитии гипоксии ребенка.
Материалы и методы
Проведен ретроспективный анализ анамнестических данных 50 новорожденных (общая выборка), находившихся на стационарном лечении в Красноярском краевом клиническом центре охраны материнства и детства (КГБУЗ «КККЦОМД»), за 2019–2020 гг.
Критерии включения:
- дети, рожденные в КГБУЗ «КККЦОМД» в 2019–2020 гг.;
- оценка по шкале Апгар ≤ 7 баллов в конце 1-й минуты;
- наличие необходимых данных соматического и акушерского анамнеза, а также сведений о вредных привычках, семейных и социальных особенностях женщин, родивших детей с асфиксией.
На основании созданной выборки были сформированы две группы новорожденных в зависимости от тяжести асфиксии при рождении. Первую группу составили 34 новорожденных ребенка, у которых при рождении была асфиксия средней степени тяжести (оценка по шкале Апгар 4–7 баллов в конце 1-й минуты жизни). Вторая группа включила 16 детей с тяжелой асфиксией при рождении (оценка по шкале Апгар 1–3 балла). Контрольную группу составили дети, сопоставимые по гестационному возрасту, без указаний на перенесенную асфиксию.
Проверка на нормальность распределения определила дальнейшие расчеты с использованием методов непараметрической статистики. Номинальные данные представлены с указанием абсолютных и относительных (%) значений. Совокупности количественных показателей описаны значениями медианы (Me) и нижнего и верхнего квартилей (Q1–Q3). Для сравнения несвязанных выборок использовался критерий χ2. Различия считались статистически значимыми при р < 0,05. Статистическая обработка данных проводилась с помощью пакета программы Microsoft Office 2021.
Результаты
Выполненный анализ позволил установить следующие особенности сформированных групп. В случае умеренной асфиксии при рождении медиана гестационного возраста составила 36 [31,3; 39] нед., а у новорожденных с тяжелой асфиксией – 33 [27,5; 37] нед. Отмечена тенденция к меньшему сроку гестации в группе детей с тяжелой асфиксией, однако достоверных различий между группами не установлено (табл. 1).
Таблица 1. Характеристика исследуемых групп
| Срок гестации, Me [Q1; Q3] | 36 [31,3; 39] | 33 [27,5; 37] |
| Нормальная масса тела, % | 53 | 31 |
| Низкая масса тела (1500–2500 г), % | 24 | 25 |
| Очень низкая масса тела (1000–1500 г), % | 12 | 13 |
| Экстремально низкой массой тела (< 1000 г), % | 12 | 31 |
| Пол (мужской/женский) | 16/18 | 8/8 |
Нормальная масса тела при рождении (по отношению к гестационному возрасту) регистрировалась в 52% случаев в группе детей с умеренной и у 31% с тяжелой асфиксией. Низкая и очень низкая масса тела при рождении в обеих группах встречалась примерно с одинаковой частотой: 24 и 25% у детей из 1-й группы и 25 и 13% из 2-й соответственно. Новорожденных с экстремально низкой массой тела при рождении установлено в 2,5 раза больше среди детей с тяжелой асфиксией – 31% против 12% в 1-й группе.
Средний возраст матерей (табл. 2) при рождении был сопоставим в обеих группах и составил 29 лет. При этом максимальный возраст матерей в обеих группах составил 39–40 лет, а значения Q3 приближались к возрасту поздней беременности – 33,5 года в обеих группах.
Таблица 2. Возраст матерей в исследуемых группах
| Max | 39 | 40 |
| Min | 16 | 18 |
| Me [Q1; Q3] | 29 [24,5; 33,5] | 32 [23,5; 33,5] |
Первоначально в работе рассмотрены факторы риска асфиксии новорожденных в общей выборке вне зависимости от степени тяжести асфиксии, и проведено сравнение с группой детей, родившихся без асфиксии (рис. 1). Выполненный сравнительный анализ позволил установить следующее. Доля курящих женщин, дети которых родились с асфиксией, составила 18% без достоверных различий с контролем. Гинекологические проблемы (воспалительные и невоспалительные болезни женских тазовых органов в период, предшествующий настоящей беременности) имели 26% женщин целевой выборки против 47% в контроле (p < 0,05). Случаи отягощенного акушерского анамнеза с медицинскими абортами (более 2 до наступления настоящей беременности) были сопоставимы и составили 30 и 32% соответственно. Антенатальная гибель плода отмечена у 7 женщин (14%), родивших детей с асфиксией, против 1 случая (5%) в контрольной группе. Данные об экстракорпоральном оплодотворении имелись только в целевой выборке женщин и отсутствовали в контроле. Особое внимание заслуживает оценка беременности, которая характеризовалась статистически значимым увеличением диагностированной фетоплацентарной недостаточности у женщин, дети которых родились с асфиксией, – 32% против 5% в контроле (p < 0,05). Сведения об угрозе выкидыша, истмико-цервикальной недостаточности и преждевременном разрыве плодных оболочек, многои маловодии были сопоставимы.
Рисунок 1. Факторы риска в исследуемых группах
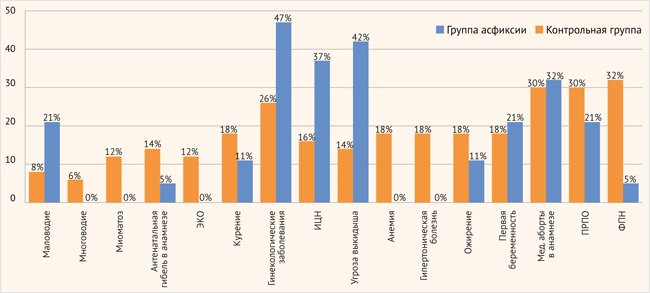
ЭКО – экстракорпоральное оплодотворение; ИЦН – истмико-цервикальная недостаточность;
ПРПО – преждевременный разрыв плодных оболочек; ФПН – фетоплацентарная недостаточность.
Последующая оценка материнских факторов риска развития асфиксии проводилась между рассматриваемыми 1-й и 2-й группами детей (с учетом степени тяжести асфиксии при рождении) (рис. 2). Результаты показали следующее. Во 2-й группе детей с тяжелой асфиксией при рождении к значимым неблагоприятным антенатальным факторам отнесены более частые материнские случаи ожирения (p < 0,05) и гипертонической болезни, указания на экстракорпоральное оплодотворение и первую беременность – 19 и 38% соответственно (против 9 и 19% в 1-й группе). Угроза невынашивания беременности также преобладала у женщин, чьи дети родились с тяжелой асфиксией, – 25% против 9% в группе умеренной асфиксии.
Рисунок 2. Антенатальные факторы риска асфиксии
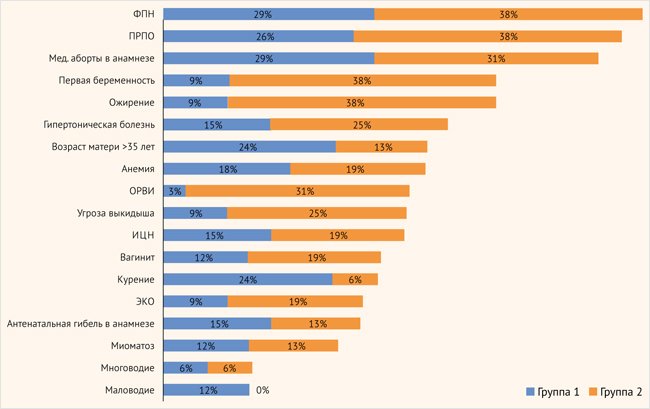
ЭКО – экстракорпоральное оплодотворение; ИЦН – истмико-цервикальная недостаточность; ПРПО – преждевременный разрыв плодных оболочек;
ФПН – фетоплацентарная недостаточность; ОРВИ – острая респираторная вирусная инфекция.
Обращает на себя внимание достоверное превышение эпизодов ОРВИ во второй половине беременности у 31% матерей новорожденных 2-й группы и 3% в 1-й. Частота встречаемости таких факторов риска, как гемодинамические нарушения плода (по данным пренатального скрининга) и медицинские аборты в анамнезе были сопоставимы в рассматриваемых группах.
Наряду с проведением сравнительного анализа причинных аспектов, неблагоприятно влияющих на антенатальное развитие плода, между рассматриваемыми группами изучены структура и соотношение этих факторов риска (рис. 3 и 4).
Рисунок 3. Соотношение факторов риска в группе умеренной асфиксии (n = 34)
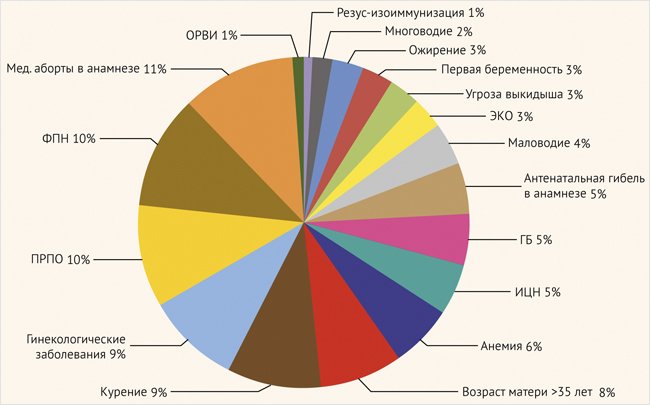
ЭКО – экстракорпоральное оплодотворение; ИЦН – истмико-цервикальная недостаточность; ПРПО – преждевременный разрыв плодных оболочек;
ФПН – фетоплацентарная недостаточность; ОРВИ – острая респираторная вирусная инфекция; ГБ – гипертоническая болезнь.
Рисунок 4. Соотношение факторов риска в группе тяжелой асфиксии (n = 16)
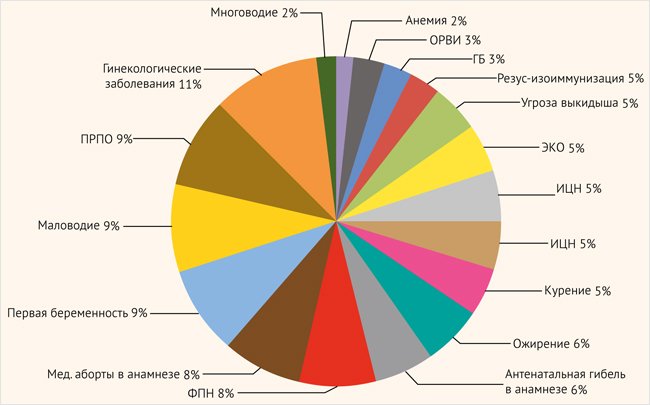
ЭКО – экстракорпоральное оплодотворение; ИЦН – истмико-цервикальная недостаточность; ПРПО – преждевременный разрыв плодных оболочек;
ФПН – фетоплацентарная недостаточность; ОРВИ – острая респираторная вирусная инфекция; ГБ – гипертоническая болезнь.
При оценке интранатальных факторов в отношении риска развития асфиксии у новорожденного обращено внимание на следующие события (рис. 5). В группе детей с тяжелой асфиксией способ родоразрешения с помощью кесарева сечения отмечен в 50% случаев (экстренное кесарево сечение – 37%, плановое – 13%); в группе новорожденных с умеренной асфиксией потребность в проведении оперативного родоразрешения составила 31% (экстренное кесарево сечение потребовалось в 28%, плановое – только в 3% случаев).
Рисунок 5. Способы родоразрешения в группах умеренной и тяжелой асфиксии
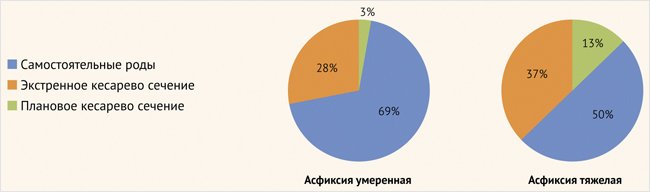
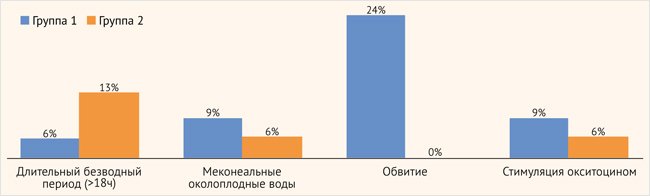
К важным маркерам неблагоприятного течения интранатального периода относятся удлинение безводного периода (более 18 ч), характер околоплодных вод, обвитие пуповиной, стимуляция окситоцином [18]. Сравнительный анализ групп показал следующее (рис. 6). У детей с тяжелой асфиксией длительный безводный период регистрировался в 13% случаев против 6% новорожденных с умеренной асфиксией. Мекониальные околоплодные воды как маркер перенесенной гипоксии плода отмечались в рассматриваемых группах с примерно одинаковой частотой (6 и 9% случаев соответственно). Обвитие пуповиной зарегистрировано только у новорожденных с умеренной асфиксией при рождении и составило 24%. Стимуляция окситоцином приводит к чрезмерной маточной активности, что значительно нарушает маточно-плацентарный кровоток и приводит к внутриутробной гипоксии [15, 19]. Стимуляция окситоцином в интранатальном периоде использовалась в 9% в 1-й группе и в 6% во 2-й.
Рисунок 6. Особенности интранатального периода у детей с асфиксией при рождении
Заключение
Понимание процессов развития гипоксии плода, а также нарушений функционирования системы «мать – плацента – плод» является важным вопросом современной перинатологии.
Основным антенатальным фактором риска, который вносит значимый вклад в развитие асфиксии новорожденных, является фетоплацентарная недостаточность, установленная в 32% случаев, что достоверно превысило показатель контрольной группы. Различные гинекологические и экстрагенитальные заболевания матери, патогенетическим звеном которых является поражение сосудов с нарушением функционирования системы «мать – плацента – плод», являются типичной реакцией плаценты на неблагоприятные воздействия и представляют механизм реализации данного фактора риска.
К факторам с негативным влиянием на плод в антенатальном периоде и определяющим более тяжелое течение асфиксии следует отнести преждевременный разрыв плодных оболочек, ожирение, первую беременность (38%), медицинские аборты в анамнезе и ОРВИ во время беременности (31%).
В интранатальном периоде факторами риска развития тяжелой асфиксии являются длительный безводный период (13%) и стимуляция окситоцином (6%).
К относительно модифицируемым (управляемым факторам риска) можно отнести медицинские аборты в анамнезе, анемию, ожирение, гипертоническую болезнь, курение.
Представленные данные актуализируют мультифакторность такого состояния, как асфиксия при рождении, подтверждают необходимость более пристального внимания к состоянию здоровья женщин репродуктивного возраста (профилактика и эффективное лечение гинекологической патологии, ожирения и гипертонической болезни, отказ от курения), обосновывают важность оптимизации наблюдения за женщинами с рассмотренными факторами риска в период беременности и родов, указывают на значительную долю неблагоприятных предикторов асфиксии, которые имеют управляемый характер, а значит, способны предотвратить развитие тяжелых гипоксических последствий у ребенка.
Список литературы / References
- Шилова Н.А., Харламова Н.В., Андреев А.В., Межинский С.С., Панова И.А., Дудов П.Р. Частота асфиксий и объем оказания реанимационной помощи новорожденным в родильном зале. Неонатология: новости, мнения, обучение. 2020;8(2):47–53. doi: 10.33029/2308-2402-2020-8-2-47-53. / Shilova N.A., Kharlamova N.V., Andreev A.V., Mezhinsky S.S., Panova I.A., Dudov P.R. Frequency of perinatal asphyxia and volume of provision of care to newborns in the delivery room. Neonatology: News, Opinions, Training. 2020;8(2):47–53. (In Russ.) doi: 10.33029/2308-2402-2020-8-2-47-53.
- Wardinger J.E., Ambati S. Placental Insufficiency. Treasure Island (FL): StatPearls Publishing; 2022. Available at: https://www.ncbi.nlm.nih.gov/.
- Анурьев А.М., Горбачев В.И. Гипоксически-ишемические поражения головного мозга у недоношенных новорожденных. Журнал неврологии и психиатрии им. С.С. Корсакова. 2019;119(8‑2):63–69. doi: 10.17116/jnevro201911908263. / Anuriev A.M., Gorbachev V.I. Hypoxic-ischemic brain damage in premature newborns. Zhurnal Nevrologii i Psikhiatrii imeni S.S. Korsakova. 2019;119(8‑2):63–69. (In Russ.) doi: 10.17116/jnevro201911908263.
- Mazarico E., Molinet-Coll C., Martinez-Portilla R.J., Figueras F. Heparin therapy in placental insufficiency: Systematic review and meta-analysis. Acta Obstet Gynecol Scand. 2020;99(2):167–174. doi: 10.1111/aogs.13730.
- Mehar M.F., Khan M.A., Saleem R., Zafar F., Naqqash A.B., Shahid S., Hassan R. Risk factors of perinatal asphyxia at Nishtar Hospital Multan. Prof Med J. 2020;27(3):487–492. doi: 10.29309/TPMJ/2020.27.3.3176.
- Карелина О.Б., Артымук Н.В. Факторы риска асфиксии новорожденных у женщин с ожирением. Фундаментальная и клиническая медицина. 2016;1(2):6–11. Режим доступа: https://fcm.kemsmu.ru/. / Karelina O.B., Artymuk N.V. Risk factors for neonatal asphyxia in obese women. Fundamental and Clinical Medicine. 2016;1(2):6–11. (In Russ.) Available at: https://fcm.kemsmu.ru/.
- Pintican D., Poienar A.A., Strilciuc S., Mihu D. Effects of maternal smoking on human placental vascularization: A systematic review. Taiwan J Obstet Gynecol. 2019;58(4):454–459. doi: 10.1016/j.tjog.2019.05.004.
- Ducsay C.A., Goyal R., Pearce W.J., Wilson S., Hu X.Q., Zhang L. Gestational Hypoxia and Developmental Plasticity. Physiol Rev. 2018;98(3):1241–1334. doi: 10.1152/physrev.00043.2017.
- Gomella T., Eyal F.G., Bany-Mohammed F. (eds.). Gomella’s Neonatology: Management, Procedures, On-Call Problems, Diseases, and Drugs. 8th ed. McGraw Hill; 2020.
- Yung H.W., Cox M., Tissot van Patot M., Burton G.J. Evidence of endoplasmic reticulum stress and protein synthesis inhibition in the placenta of non-native women at high altitude. FASEB J. 2012;26(5):1970–1981. doi: 10.1096/fj.11-190082.
- Herrera C.A., Silver R.M. Perinatal Asphyxia from the Obstetric Standpoint: Diagnosis and Interventions. Clin Perinatol. 2016;43(3):423–438. doi: 10.1016/j.clp.2016.04.003.
- Pintican D., Poienar A.A., Strilciuc S., Mihu D. Effects of maternal smoking on human placental vascularization: A systematic review. Taiwan J Obstet Gynecol. 2019;58(4):454–459. doi: 10.1016/j.tjog.2019.05.004.
- Wong S.F., Chow K.M., Leung T.N., Ng W.F., Ng T.K., Shek C.C. et al. Pregnancy and perinatal outcomes of women with severe acute respiratory syndrome. Am J Obstet Gynecol. 2004;191(1):292–297. doi: 10.1016/j.ajog.2003.11.019.
- Yang Z., Wang M., Zhu Z., Liu Y. Coronavirus disease 2019 (COVID-19) and -pregnancy: a systematic review. J Matern Fetal Neonatal Med. 2022;35(8):1619–1622. doi: 10.1080/14767058.2020.1759541.
- Кузнецов П.А., Козлов П.В. Гипоксия плода и асфиксия новорожденного. Лечебное дело. 2017;(4):9–15. Режим доступа: https://www.elibrary.ru/. / Kuznetsov P.A., Kozlov P.V. Fetal hypoxia and neonatal asphyxia. Lechebnoe Delo. 2017;(4):9–15. (In Russ.) Available at: https://www.elibrary.ru/.
- Torres-Muñoz J., Rojas C., Mendoza-Urbano D., Marín-Cuero D., Orobio S., Echandía C. Risk factors associated with the development of perinatal asphyxia in neonates at the Hospital Universitario del Valle, Cali, Colombia, 2010–2011. Biomedica. 2017;37(1 Suppl.):51–56. (In Spanish) doi: 10.7705/biomedica.v37i1.2844.
- Исенова С.Ш., Бодыков Г.Ж., Локшин В.Н., Джусубалиева Т.М., Байкошкарова С.Б., Карибаева Ш.К. и др. Особенности течения раннего неонатального периода новорожденных после применения ЭКО. Репродуктивная медицина. 2020;(2):22–27. doi: 10.37800/RM2020-1-12. / Isenova S.Sh., Bodykov G.Zh., Lokshin V.N., Dzhusubalieva T.M., Baikoshkarova S.B., Karibaeva Sh.K. Features of the early neonatal period of newborns after IVF. Reproductive Medicine. 2020;(2):22–27. (In Russ.) doi: 10.37800/RM2020-1-12.
- Haliti A., Mustafa L., Bexheti S., Islami D., Bozalija A., Shabani R., Islami H. In Vitro Action of Meconium on Bronochomotor Tonus of Newborns with Meconium Aspiration Syndrome. Open Access Maced J Med Sci. 2018;6(6):992–996. doi: 10.3889/oamjms.2018.244.
- Nam N.H., Sukon P. Risk factors associated with stillbirth of piglets born from oxytocin-assisted parturitions. Vet World. 2020;13(10):2172–2177. doi: 10.14202/vetworld.2020.2172-2177.